痒,可能是人类最矛盾的感觉体验。它微不足道,却能把人逼疯——慢性痒患者的生活质量评分与慢性痛患者相当。它令人抓狂,挠一下却又无比舒爽——那种"解了"的快感让人欲罢不能。更奇怪的是,看别人挠痒,你也会跟着痒起来。
但科学家花了一百年才搞清楚:痒到底是怎么回事?
一个被误解了百年的感觉
直到21世纪初,医学教科书对痒的定义还很模糊:痒是"轻度的疼痛"。这个观念可以追溯到20世纪初德国生理学家Max von Frey提出的"强度理论"——认为同一根神经纤维传导不同强度的刺激,弱刺激产生痒,强刺激产生痛。
这个理论统治了近一个世纪。它解释了很多现象:为什么挠痒(产生疼痛)能止痒?为什么吗啡这类强效止痛药反而会让人更痒?为什么先天对疼痛不敏感的人也不会感到痒?
但漏洞也很明显。抗组胺药能缓解蚊虫叮咬引起的痒,却对大多数慢性痒无效。临床上,很多严重瘙痒患者用止痛药毫无效果。更重要的是,如果痒只是轻度疼痛,为什么我们的体验如此不同?痛让我们退缩,痒却让我们…想挠。
争论的焦点在于:痒和痛是共用一条神经线路,还是各有专属通道?
2007年:一个基因改变了认知
转机出现在2007年。华盛顿大学医学院的陈宙峰(Zhou-Feng Chen)团队在《Nature》发表了一篇论文,宣布发现了第一个"痒基因"——胃泌素释放肽受体(Gastrin-Releasing Peptide Receptor,简称GRPR)。
这个发现的过程堪称教科书级别的科学探险。陈宙峰团队当时正在研究脊髓中与疼痛相关的基因,他们注意到一个奇怪的现象:GRPR基因在脊髓背角有表达,但敲除这个基因的小鼠对疼痛刺激的反应完全正常。
那这个基因是干什么的?研究团队决定测试一下痒觉。他们给正常小鼠和GRPR敲除小鼠皮下注射各种致痒物质——组胺、氯喹、血清素等。结果令人震惊:正常小鼠疯狂抓挠,而GRPR敲除小鼠几乎无动于衷。
这个实验证明了两件事:第一,GRPR是痒觉传递的关键分子;第二,痒觉和痛觉确实是两条独立的神经线路。
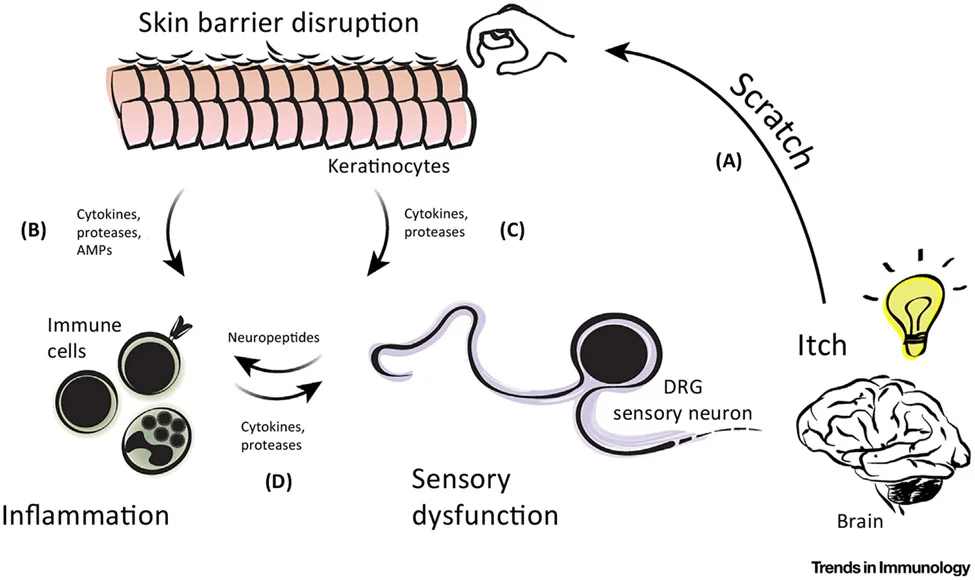
图片来源:PMC/NIH - The Itch–Scratch Cycle: A Neuroimmune Perspective
2009年,陈宙峰团队进一步做了更极端的实验:他们用毒素特异性地杀死脊髓中表达GRPR的神经元。结果,这些小鼠对各种致痒物质的抓挠反应完全消失,但疼痛感知完全保留。这彻底终结了百年争议:痒不是轻度的痛,它有自己专属的神经通路。
两条平行的痒觉高速公路
但事情没那么简单。科学家很快发现,痒觉本身就有多条通路。
最先被研究的是组胺依赖性痒觉通路。组胺是肥大细胞释放的一种化学物质,也是蚊虫叮咬后引起瘙痒的主要元凶。当组胺激活皮肤上的H1/H4受体后,信号沿着一种特殊的神经纤维——机械不敏感C纤维(CMi)——传递。这些纤维有一个特点:传导速度极慢,每秒仅0.5米,分支范围极广。这解释了为什么组胺引起的痒往往范围很大,还会伴随周围皮肤发红(神经源性炎症)。
但临床医生早就发现,抗组胺药对许多瘙痒完全无效。比如抗疟疾药物氯喹引起的剧烈瘙痒,抗组胺药毫无作用。这是为什么?
2011年,美国国立卫生研究院(NIH)的研究团队找到了答案。他们发现氯喹激活的是另一类受体——MrgprA3(小鼠)/MrgprX1(人类)。这是Mas相关G蛋白偶联受体家族的成员,专门负责非组胺依赖的痒觉信号。
两条通路的差异不止于此。组胺通路主要涉及TRPV1离子通道,而氯喹通路则依赖TRPA1。在脊髓层面,它们激活的神经元群体虽然都表达GRPR,但上游信号输入不同。这解释了为什么有些痒抗组胺药有效,有些无效。
timeline
title 两种痒觉通路的对比
section 组胺依赖通路
外周 : 组胺激活H1/H4受体
离子通道 : TRPV1介导信号
神经纤维 : 机械不敏感C纤维(CMi)
特点 : 传导慢、范围广、伴发红
section 非组胺依赖通路
外周 : 氯喹激活MrgprA3/X1
离子通道 : TRPA1介导信号
神经纤维 : 多模式C纤维
特点 : 抗组胺药无效、局限痒感
痒觉如何"爬"进大脑
找到了脊髓中的痒觉中继站,下一个问题是:痒觉信号如何从脊髓传到大脑?
2017年,中科院神经科学研究所孙衍刚团队在《Science》发表了一篇里程碑式的论文。他们发现,脊髓中表达GRPR的神经元并不直接投射到大脑,而是先激活另一群投射神经元,这些神经元的轴突延伸到脑干的一个结构——臂旁核(Parabrachial Nucleus)。
臂旁核是什么?它是脑干中的一个"感觉信息枢纽",负责整合来自全身的各种感觉信号,然后传递给丘脑和更高级的大脑皮层。孙衍刚团队的实验表明,阻断脊髓-臂旁核通路,小鼠对致痒物质的抓挠反应完全消失,但对疼痛刺激的反应正常。
sequenceDiagram
participant Skin as 皮肤感受器
participant DRG as 背根神经节
participant SC as 脊髓GRPR+神经元
participant PBN as 臂旁核
participant Thalamus as 丘脑
participant Cortex as 大脑皮层
Skin->>DRG: 致痒物质激活<br/>组胺/Mrgpr受体
DRG->>SC: 释放GRP肽
SC->>PBN: 兴奋性信号传递
PBN->>Thalamus: 痒觉信号上传
Thalamus->>Cortex: 产生痒的主观体验
这个发现的意义在于:它绘制了痒觉从中枢神经系统传向大脑的第一张"高速公路地图"。从此,痒不再是一个模糊的感觉现象,而是一条可以追踪的神经回路。
为什么挠痒会"爽"?
这是痒觉最迷人的一面:挠痒不仅止痒,还会产生一种独特的快感。
2013年,美国维克森林大学的研究团队用功能性磁共振成像(fMRI)扫描了正在挠痒的人的大脑。结果发现,挠痒激活了大脑的奖赏系统——包括纹状体和腹侧被盖区(VTA),这些区域正是多巴胺神经元聚集的地方。
更精细的研究揭示了时间上的巧合:挠痒动作开始后约1秒,中脑腹侧被盖区的多巴胺神经元开始兴奋。这些神经元将信号传递到伏隔核,产生那种"好爽"的感觉。这解释了为什么挠痒会让人上瘾——某种程度上,它和吃美食、赢钱激活的是同一套神经回路。
timeline
title 挠痒时的大脑活动时序
section 皮肤层面
0s : 挠痒动作开始<br/>激活伤害性感受器
section 脊髓层面
~0.05s : 痒觉信号被疼痛信号抑制<br/>GRPR神经元活动下降
section 大脑层面
~0.5s : 奖赏系统开始激活<br/>纹状体血流量增加
~1.0s : 多巴胺释放<br/>产生"解痒"快感
但这又引出一个悖论:如果挠痒产生快感,为什么我们不会一直挠下去?
2025年2月发表的一项研究给出了答案。匹兹堡大学的研究团队发现,挠痒激活的伤害性神经元会释放一种叫做P物质的神经肽,这种肽作用于肥大细胞,促使它们释放更多炎症介质。这形成了一个恶性循环——挠痒缓解痒觉的同时,也在制造更多的痒。
2025年的意外发现:挠痒竟然有保护作用?
长期以来,医学界对"挠痒"的态度是负面的:它损伤皮肤、加重炎症、可能导致感染。但2025年1月发表在《Science》的一项研究彻底颠覆了这个认知。
匹兹堡大学D.H. Kaplan团队的研究发现,挠痒虽然会加重皮肤炎症,但同时也能显著降低皮肤表面金黄色葡萄球菌的数量。机制是这样的:挠痒激活的伤害性神经元释放P物质,P物质作用于肥大细胞的MrgprB2受体,促使肥大细胞释放更多TNF等炎症因子,这些因子招募中性粒细胞到皮肤表面,发挥抗菌作用。
这个发现从进化角度解释了痒-抓反射的存在意义:在远古环境中,皮肤上的痒往往是寄生虫或病原体入侵的信号。挠痒一方面驱除这些入侵者,另一方面激活局部免疫防御,形成双重保护。在现代环境中,这个原本有益的机制可能过度激活,导致慢性瘙痒和皮肤病变。
传染性痒:为什么看别人挠你也想挠
痒还有一个奇特之处:它会传染。看别人挠痒,或者仅仅看到与痒相关的图片,你也会莫名其妙地感到痒。
2012年,英国赫尔大学的研究团队首次用实验证实了这一现象。他们让志愿者观看人们挠痒的视频,结果发现64%的志愿者报告自己也开始痒,而且确实开始抓挠。对照组观看人们只是敲打手臂的视频,则没有这种效应。
fMRI研究揭示了背后的神经机制。当人们观看挠痒视频时,大脑中几个关键区域被激活:前扣带回皮层(与共情相关)、岛叶(处理主观感受)、运动皮层(准备执行抓挠动作)。有趣的是,这些区域也是"传染性打哈欠"时激活的区域。
2017年,华盛顿大学的研究团队进一步发现,传染性痒涉及一条从视交叉上核到室旁核再到臂旁核的神经通路。这条通路与直接痒觉通路部分重叠,可能解释了为什么视觉刺激可以绕过外周感受器,直接激活痒觉体验。
痒觉研究的未来
从2007年GRPR的发现到现在,痒觉研究经历了翻天覆地的变化。曾经被认为是"轻度疼痛"的感觉,现在被确认为一套独立的、复杂的神经免疫系统。
在治疗层面,针对痒觉特异分子的药物正在研发中。比如针对IL-31受体的尼莫利珠单抗(Nemolizumab)已经在临床试验中显示出对特应性皮炎相关瘙痒的显著效果。针对GRPR的拮抗剂也在研发中。
但痒觉仍然有很多未解之谜。为什么痒觉没有像痛觉那样的"先天性不敏感"案例?痒觉的编码是"特异性通路"还是"群体编码"?不同类型的痒(机械痒、化学痒、神经病理性痒)的大脑处理有何不同?
这些问题不仅关乎科学理解,更关乎数百万慢性瘙痒患者的福祉。当我们终于开始理解"痒"这个看似微不足道的感觉时,才发现它背后隐藏的是神经科学、免疫学和进化生物学的复杂交响。
参考资料
- Sun YG, Chen ZF. A gastrin-releasing peptide receptor mediates the itch sensation in the spinal cord. Nature. 2007;448(7154):700-703.
- Liu Q, et al. Sensory neuron-specific GPCRs Mrgprs are itch receptors mediating chloroquine-induced pruritus. Cell. 2009;139(7):1353-1365.
- Mu D, et al. A central neural circuit for itch sensation. Science. 2017;357(6352):695-699.
- Liu AW, et al. Scratching promotes allergic inflammation and host defense via neurogenic mast cell activation. Science. 2025;387(6733):adn9390.
- Papoiu AD, et al. Brain’s reward circuits mediate itch relief. A functional MRI study of successful scratching. J Invest Dermatol. 2013;133(12):2834-2841.
- Mu D, Sun YG. Central circuit mechanisms of itch. Nat Commun. 2020;11(1):3052.
- Akiyama T, Carstens E. Neural processing of itch. Neuroscience. 2013;250:697-714.
- Dong X, Dong X. Peripheral and central mechanisms of itch. Neuron. 2018;98(3):482-494.
- LaMotte RH, et al. Neuronal and behavioral mechanisms of itch. Nat Rev Neurosci. 2020;21(8):437-451.
- Sun S, et al. Leaky gate model: intensity-dependent coding of pain and itch in the spinal cord. Neuron. 2019;102(6):1143-1156.