演讲前几分钟,腹部开始隐隐作痛;重大考试当天,胃里翻江倒海;收到那封重要邮件后,一阵尖锐的痉挛袭来。这些体验如此普遍,以至于我们习以为常。但为什么情绪波动会精准地"打击"胃部?答案藏在一条连接大脑与胃肠的神秘通道里——科学家称之为脑肠轴(Gut-Brain Axis)。
这不是比喻。你的胃肠道里真的有一个"大脑",它拥有约5亿个神经元,比脊髓还多,能够独立运作,却也时刻与颅脑保持密切联络。当压力来袭,这条双向高速路上会掀起一场神经风暴,最终在你的胃里引爆。
肠道里的"第二大脑"
1998年,哥伦比亚大学的神经科学家Michael Gershon出版了《第二大脑》(The Second Brain)一书,系统阐述了一个革命性观点:胃肠道的神经系统复杂到足以被称为独立的"大脑"。
这个被称为肠神经系统(Enteric Nervous System,ENS)的神经网络,由两层神经细胞组成:肌间神经丛(Auerbach神经丛)位于肠道的环形肌和纵行肌之间,控制肠道运动;黏膜下神经丛(Meissner神经丛)位于黏膜下层,调节分泌和血流。整个系统从食管一直延伸到直肠,形成一条完整的神经管道。
肠神经系统的独立性强得惊人。即便切断迷走神经——连接大脑与肠道的主要通道——肠道仍能完成基本的消化功能。它有自己的感觉神经元、中间神经元和运动神经元,能够自主整合信息并做出反应。Gershon指出,这种进化设计让"颅脑不必亲自处理消化这件脏活"。
更令人惊讶的是神经递质的分布。肠神经系统使用超过30种神经递质,与大脑使用的基本相同。约95%的血清素(5-HT)在肠道产生,主要储存于肠嗜铬细胞和肠神经元中;多巴胺的一半也来自肠道。这些"快乐物质"在胃肠里的角色并非调节情绪,而是控制肠蠕动、分泌和血流——但它们的存在解释了为什么抗抑郁药(SSRIs)常常引起胃肠道副作用。
迷走神经:一条不对称的高速公路
肠神经系统并非与世隔绝。它通过迷走神经与大脑保持实时联络。迷走神经是第10对脑神经,从脑干延伸至腹腔,分支连接心脏、肺和整个消化道。
关键数据颠覆直觉:迷走神经中约80%的纤维是传入纤维(从肠到脑),只有20%是传出纤维(从脑到肠)。这意味着,迷走神经更像是一条汇报通道——肠道持续向大脑发送状态报告,而非大脑对肠道发号施令。
当肠道感到"不安"——炎症、扩张、化学变化——信号沿迷走神经传至脑干的孤束核,再投射到大脑皮层和边缘系统,最终可能引发情绪变化。Johns Hopkins大学的研究发现,肠易激综合征(IBS)患者的肠神经系统持续发送"麻烦信号"到大脑,这可能是他们更容易出现焦虑和抑郁的原因之一。
压力按下"紧急按钮":HPA轴启动
当大脑感知到威胁——无论是真实的危险还是想象中的压力——杏仁核(Amygdala)首先被激活。这个杏仁状的脑区是情绪处理的中枢,尤其在恐惧和焦虑反应中扮演核心角色。
杏仁核向位于大脑底部的下丘脑发送警报。下丘脑随即启动HPA轴(下丘脑-垂体-肾上腺轴)——身体应对压力的核心内分泌系统:
- 下丘脑释放促肾上腺皮质激素释放激素(CRH)
- CRH通过门静脉到达垂体前叶,刺激释放促肾上腺皮质激素(ACTH)
- ACTH经血液循环到达肾上腺皮质,促使皮质醇分泌
皮质醇是压力荷尔蒙,它的作用遍及全身。但CRH本身也对胃肠系统有直接影响——研究表明,静脉注射CRH可以诱发正常人肠道运动改变,而肠易激综合征患者的反应更为剧烈。
timeline
title 压力引发的神经内分泌反应时序
section 感知阶段
0s : 杏仁核感知威胁<br/>情绪信号整合
section 神经反应
~1s : 下丘脑激活<br/>交感神经兴奋
~2s : 迷走神经张力下降<br/>胃肠蠕动减缓
section 内分泌反应
~10s : CRH释放<br/>HPA轴启动
~分钟级 : ACTH分泌<br/>皮质醇水平上升
section 胃肠效应
~分钟级 : 胃酸分泌改变<br/>黏膜保护减弱
~持续 : 内脏敏感性增高<br/>疼痛感知放大
交感神经系统的"战或逃"响应
与HPA轴同步启动的是交感神经系统。这是更快速的反应通道,负责经典的"战或逃"(Fight-or-Flight)反应。
交感神经兴奋后,身体发生一系列变化:心率加快、血压升高、支气管扩张、瞳孔放大。同时,血液从消化系统重新分配到骨骼肌和心脏——这本是为搏斗或逃跑做准备。研究显示,急性压力下,胃肠道的血流量可显著下降。
胃肠道的平滑肌受到双重打击:交感神经释放的去甲肾上腺素直接抑制肠蠕动;副交感神经(迷走神经)的张力下降,进一步削弱了消化功能。结果就是:胃排空延迟、肠道蠕动紊乱,你会感到腹胀、消化不良,甚至恶心。
与此同时,压力还会影响胃酸分泌。虽然急性压力可能通过交感神经抑制胃酸分泌(作为保护机制),但慢性压力往往导致胃酸分泌增加,同时削弱胃黏膜的保护屏障。UniCamillus大学的Giovanni Leonetti教授指出,当压力和焦虑水平很高时,酸性消化液的分泌会增加,而保护胃黏膜的黏液和前列腺素会减少——这正是压力性胃炎的病理基础。
内脏高敏感性:放大器被调到最大
压力导致胃痛还有一个关键机制:内脏高敏感性(Visceral Hypersensitivity)。
正常情况下,胃肠道的适度扩张或收缩不会引起疼痛。但在压力状态下,中枢神经系统对内脏信号的处理方式发生了改变。影像学研究显示,肠易激综合征患者在接受直肠扩张刺激时,大脑中与疼痛处理相关的区域(如前扣带皮层、岛叶、杏仁核)表现出异常激活模式——他们的大脑对内脏信号的"放大器"被调高了。
这种中枢敏化(Central Sensitization)意味着:同样的胃肠道刺激,在压力状态下被解读为更强烈的疼痛。这就是为什么紧张时,普通的胃部不适可能感觉像剧烈的绞痛。
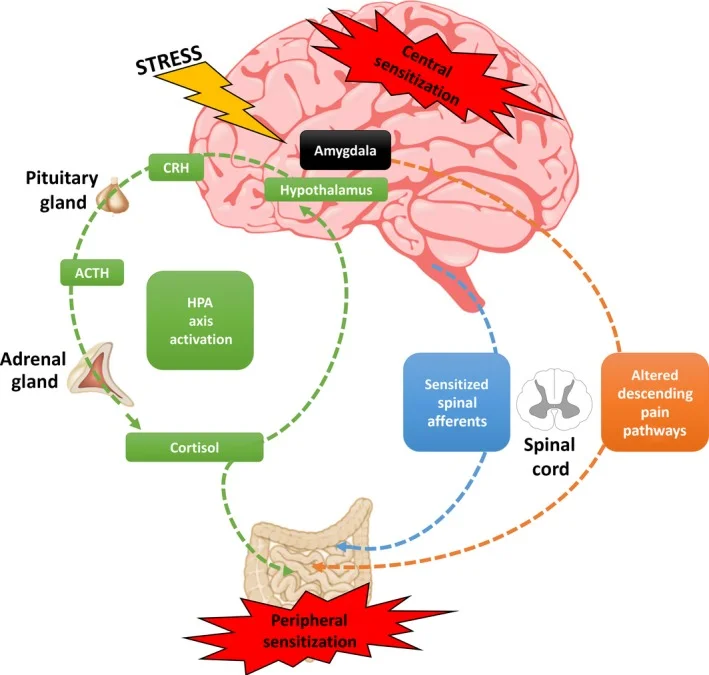
图片来源: PMC / NCBI - 中枢和外周疼痛敏化机制示意图。HPA轴被压力激活,下丘脑分泌CRH进入垂体门脉系统,刺激垂体释放ACTH。肾上腺皮质释放皮质醇,可直接激活胃肠道内的免疫细胞和外周初级传入纤维,促进外周敏化。皮质醇与杏仁核结合则进一步促进CRH分泌,形成中枢敏化。
临床证据:数字背后的真相
流行病学数据证实了压力与胃肠症状的紧密关联。一项发表于2022年的研究显示,功能性消化不良患者中,50.4%伴有焦虑,42.4%伴有抑郁——显著高于健康对照组的13.3%和6.66%。肠易激综合征患者中,焦虑和抑郁的共病率在20-60%之间。
更具说服力的是CRH实验。日本学者Fukudo等人给健康志愿者和IBS患者静脉注射CRH,结果两组都出现了肠道运动改变,但IBS患者的反应更为强烈,腹痛症状持续时间更长。这表明,IBS患者的"脑-肠"系统对压力信号存在过度反应。
高达30-40%的人群在某个时点会出现功能性胃肠问题——这些疾病没有明显的结构性异常,却伴随真实的痛苦症状。它们的共同特征是:脑肠轴的功能紊乱。
从机制到应对
理解了紧张导致胃痛的神经科学机制,应对策略便有了科学依据。
心理干预:认知行为疗法(CBT)已被证实能改善功能性胃肠病患者的症状。其机制正是通过调节大脑对压力的处理方式,间接影响脑肠轴的功能。
迷走神经刺激:深呼吸、冥想等放松技术可以增加迷走神经张力,激活副交感神经系统,帮助胃肠功能恢复。
生活方式调整:少食多餐、充分咀嚼、避免立即躺下——这些看似简单的建议,实际上是在减轻肠神经系统的负担,让它能更好地应对压力带来的干扰。
当紧张时胃痛不再是偶尔的困扰,而是频繁出现的症状时,可能需要专业的医学评估。功能性消化不良、肠易激综合征等疾病虽然"功能性"——没有器质性病变——但痛苦是真实的,治疗也是必要的。
引用来源
- Gershon MD. The Second Brain: A Groundbreaking New Understanding of Nervous Disorders of the Stomach and Intestine. HarperCollins, 1998.
- Johns Hopkins Medicine. The Brain-Gut Connection. https://www.hopkinsmedicine.org/health/wellness-and-prevention/the-brain-gut-connection
- Harvard Health Publishing. The gut-brain connection. 2023. https://www.health.harvard.edu/diseases-and-conditions/the-gut-brain-connection
- Breit S, Kupferberg A, Rogler G, et al. Vagus Nerve as Modulator of the Brain–Gut Axis in Psychiatric and Inflammatory Disorders. Frontiers in Neuroscience, 2018.
- Moloney RD, O’Leary OF, Felice D, et al. Stress and the Microbiota–Gut–Brain Axis in Visceral Pain. International Journal of Clinical Pharmacology, 2016.
- Fukudo S, Nomura T, Muranaka M, et al. Impact of corticotropin-releasing hormone on gastrointestinal motility. Gut, 1997.
- Carabotti M, Scirocco A, Maselli MA, et al. The gut-brain axis: interactions between enteric microbiota, central and enteric nervous systems. Annals of Gastroenterology, 2015.
- Scientific American. Think Twice: How the Gut’s “Second Brain” Influences Mood and Well-Being. 2010.
- UniCamillus University. Stress-induced gastritis: when stress affects the stomach. 2024.
- Cleveland Clinic. What Is the Gut-Brain Connection? https://my.clevelandclinic.org/health/body/the-gut-brain-connection