1879年的某个傍晚,约翰·霍普金斯大学的化学家康斯坦丁·法尔伯格在实验室工作到很晚。回家吃饭时,他发现晚餐的面包有着异常的甜味——他忘了洗手。这个疏忽让他意识到,自己手上残留的某种煤焦油衍生物竟然比糖甜数百倍。就这样,第一种人工甜味剂糖精(Saccharin)被意外发现。
一个半世纪过去了,人工甜味剂已经从实验室的偶然发现演变为一个年产值超过200亿美元的全球产业。然而,这些化合物如何在分子层面上"欺骗"我们的味觉系统、它们对代谢的影响究竟如何,直到最近十年才逐渐有了清晰的答案。
一个受体,两种蛋白,五种结合位点
人类对甜味的感知始于舌头上约一万个味蕾。每个味蕾中包含50-100个味觉受体细胞,其中专门感知甜味的细胞表面表达着一种特殊的蛋白质复合物:T1R2/T1R3受体。
这个受体属于C类G蛋白偶联受体(GPCR)家族,其结构与代谢型谷氨酸受体相似。每个亚基都包含三个主要结构域:位于细胞外的Venus Flytrap模块(VFTM)、富含半胱氨酸的结构域(CRD),以及七次跨膜结构域(TMD)。VFTM因其形似捕蝇草的开合结构而得名——当甜味分子结合时,两个"叶片"会像捕蝇草一样闭合,触发下游信号传导。
2025年发表在《Cell》上的冷冻电镜研究首次解析了人类甜味受体与阿斯巴甜和三氯蔗糖结合的高分辨率结构。研究发现,这个异源二聚体受体拥有至少五个不同的结合位点:VFTM区域可以结合糖类和阿斯巴甜,TMD区域可以结合甜蜜素和乳酸醇,而CRD区域则参与甜味蛋白的结合。
flowchart TB
subgraph T1R2["T1R2 亚基"]
VFTM2["VFTM\n(结合糖类、阿斯巴甜)"]
CRD2["CRD"]
TMD2["TMD"]
end
subgraph T1R3["T1R3 亚基"]
VFTM3["VFTM"]
CRD3["CRD\n(结合甜味蛋白)"]
TMD3["TMD\n(结合甜蜜素、乳酸醇)"]
end
VFTM2 --- VFTM3
CRD2 --- CRD3
TMD2 --- TMD3
ASP["阿斯巴甜"] --> VFTM2
SUC["三氯蔗糖"] --> VFTM2
CYC["甜蜜素"] --> TMD3
阿斯巴甜的结合方式尤其精妙。研究表明,它主要结合在T1R2亚基的VFTM口袋中,通过11个关键氨基酸残基与受体相互作用。其中,两个水分子在配体口袋中起到了桥梁作用,将阿斯巴甜的羰基与受体残基D142和L279连接起来。这种精确的分子识别解释了为什么人类能感知阿斯巴甜的甜味,而小鼠却不能——小鼠T1R2的相应位置缺少关键的氨基酸。
甜度的数量级差异
人工甜味剂最显著的特征是它们的甜度强度远超蔗糖。糖精的甜度约为蔗糖的300-700倍,阿斯巴甜约为180-200倍,而三氯蔗糖则高达600倍。更令人惊讶的是,阿德万塔梅(Advantame)的甜度可达蔗糖的20,000倍。
这种巨大的甜度差异源于受体激活效率的不同。当甜味分子与受体结合时,会诱导VFTM从"开放"构象转变为"闭合"构象。人工甜味剂往往能更高效地稳定这种闭合状态,从而触发更强的信号传导。此外,某些人工甜味剂还能与受体上的别构调节位点结合,进一步增强甜味感知。
然而,甜度强度的提升伴随着味道质量的下降。糖精和安赛蜜钾都会产生明显的苦味后味,这种金属味在浓度较高时尤为明显。研究发现,这是因为这些分子不仅能激活甜味受体,还能激活某些苦味受体(如TAS2R31)。这种多重受体的激活是许多人工甜味剂"味道不纯"的分子基础。
零卡路里的秘密
人工甜味剂能够提供甜味却不提供热量,这一特性源于它们的代谢命运。
糖精和三氯蔗糖在人体内几乎不被代谢。它们的化学结构使其能够抵抗消化酶的分解,最终以原形通过消化道排出。这意味着它们不参与葡萄糖代谢途径,也就不会产生热量。
阿斯巴甜则是一个例外。作为一种二肽衍生物(L-天冬氨酰-L-苯丙氨酸甲酯),它在体内会被酯酶水解为天冬氨酸、苯丙氨酸和少量甲醇。这些代谢产物确实会产生约4千卡/克的热量,但由于阿斯巴甜的甜度极高,达到相同甜味所需的剂量极小——一罐无糖饮料中的阿斯巴甜仅产生不到1千卡的热量,在营养标签上可以忽略不计。
胰岛素的意外响应
如果人工甜味剂不提供葡萄糖,它们是否会影响胰岛素分泌?这个问题困扰了研究者数十年。
早期的"头期胰岛素反应"(Cephalic Phase Insulin Response, CPIR)假说认为,甜味刺激会通过神经反射触发胰岛素的早期释放。然而,多项研究得出了矛盾的结论:一些实验观察到阿斯巴甜能刺激胰岛素分泌,而另一些则未发现这种效应。
2025年发表在《Cell Metabolism》上的研究为这一争议提供了重要线索。研究团队发现,阿斯巴甜能够通过迷走神经激活胰岛素分泌。当小鼠摄入含有0.15%阿斯巴甜的食物后,血浆胰岛素水平在30分钟内显著升高。更重要的是,双侧膈下迷走神经切断术完全阻断了这种胰岛素响应。
这种效应的机制与甜味受体在胃肠道的分布有关。T1R2/T1R3受体不仅存在于味蕾,还广泛分布于胃肠道的肠内分泌细胞中。当阿斯巴甜与肠道中的甜味受体结合时,可能通过神经通路向胰腺发送信号,刺激胰岛素分泌。
同一研究还发现,持续的阿斯巴甜摄入会导致小鼠出现胰岛素抵抗。在12周的喂养实验中,接受阿斯巴甜的小鼠在葡萄糖耐量试验和胰岛素耐量试验中都表现出异常。这表明,虽然人工甜味剂不直接提供葡萄糖,但它们可能通过影响胰岛素分泌和敏感性来间接影响代谢。
肠道菌群的沉默受害者
2014年发表在《Nature》上的研究首次系统性地揭示了人工甜味剂与肠道微生物之间的关系。研究团队发现,小鼠在摄入糖精、三氯蔗糖或阿斯巴甜后,出现了葡萄糖耐受不良,而这一效应伴随着肠道微生物组成的显著改变。
为了验证肠道菌群是否是这一效应的中介,研究者进行了经典的粪菌移植实验。他们将人工甜味剂喂养小鼠的肠道菌群转移给无菌小鼠,结果发现,接受"甜味剂菌群"的小鼠也出现了葡萄糖耐受不良。反过来,用抗生素清除人工甜味剂喂养小鼠的肠道菌群后,葡萄糖耐受不良的现象消失了。
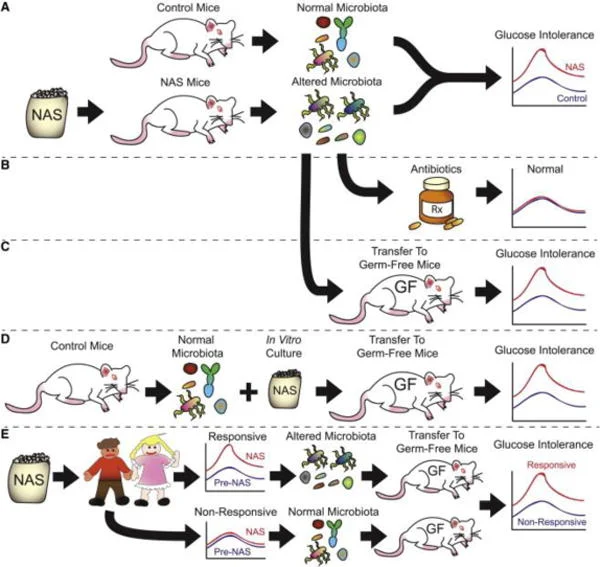
图片来源:PMC/Cell Metabolism - 实验设计示意图:人工甜味剂通过改变肠道菌群诱导葡萄糖耐受不良
研究还发现,人工甜味剂对菌群的影响存在个体差异。在人类志愿者实验中,给予糖精一周后,部分受试者出现了葡萄糖耐受不良和菌群变化,而另一部分则没有。将"响应者"和"非响应者"的粪菌分别转移给无菌小鼠后,只有接受"响应者"菌群的小鼠出现了葡萄糖耐受不良。这表明,个体的基线菌群组成可能决定了人工甜味剂对代谢的影响程度。
在分子水平上,人工甜味剂似乎会影响微生物的糖降解途径。宏基因组测序显示,甜味剂处理后,涉及多糖降解的微生物基因表达发生改变,导致短链脂肪酸的产量变化。短链脂肪酸是肠道微生物代谢膳食纤维的产物,它们不仅为结肠上皮细胞提供能量,还通过刺激GLP-1分泌来调节胰岛素敏感性。
血管炎症的新发现
2025年《Cell Metabolism》的研究还揭示了阿斯巴甜与动脉粥样硬化之间的联系。在载脂蛋白E敲除(ApoE⁻/⁻)小鼠模型中,12周的阿斯巴甜喂养显著加剧了主动脉斑块的形成和不稳定性。
机制研究发现,阿斯巴甜诱导的高胰岛素水平会上调内皮细胞中CX3CL1趋化因子的表达。CX3CL1是一种独特的趋化因子,它同时具有粘附和趋化活性,能够吸引表达CX3CR1的单核细胞/巨噬细胞向内皮细胞聚集。这些聚集的炎症细胞进入血管壁后,转化为泡沫细胞,加速动脉粥样硬化斑块的进展。
在人类和灵长类动物实验中,阿斯巴甜同样导致了胰岛素水平的升高。喂食含有0.15%阿斯巴甜食物的猴子在30分钟内血浆胰岛素水平显著增加,这一效应与小鼠实验结果一致。
安全评估的复杂图景
2023年7月,世界卫生组织下属的国际癌症研究机构(IARC)将阿斯巴甜列为"可能对人类致癌"(Group 2B)的物质。这一分类基于有限的证据,主要是观察性研究中发现的与肝癌的关联。
IARC的分类体系衡量的是危害证据的强度,而非实际风险的大小。Group 2B意味着"有一些证据表明可能致癌,但证据尚不充分"。与之形成对比的是,同一级别还包括泡菜、芦荟提取物和汽油发动机尾气。
世界卫生组织和粮农组织联合专家委员会(JECFA)在同一天发布的风险评估则更为谨慎。JECFA认为,在目前的摄入水平下,阿斯巴甜的安全性是可接受的,并维持了40毫克/千克体重的每日允许摄入量(ADI)。对于一个60千克的成年人来说,这意味着每天可以安全摄入相当于12-36罐无糖饮料中阿斯巴甜的量。
美国食品药品监督管理局(FDA)设定的阿斯巴甜ADI更为宽松,为50毫克/千克体重。FDA指出,即使是无糖饮料的重度消费者,其阿斯巴甜摄入量也很难超过这一限值。
权衡与选择
人工甜味剂的研究揭示了一个复杂的事实:这些化合物远非"无热量的糖"那么简单。它们通过与甜味受体的精确相互作用产生甜味,通过特殊的代谢路径实现零热量,但同时也可能通过神经和微生物途径影响代谢。
2024年的荟萃分析显示,用人工甜味剂替代添加糖可以在短期内减少热量摄入和体重,但对长期代谢健康的影响仍存在争议。对于糖尿病患者或需要控制血糖的人群,人工甜味剂仍是一个可行的选择——毕竟,添加糖对血糖的直接影响是明确且显著的。
最新的研究提示,不同的人工甜味剂可能有不同的生物学效应。阿斯巴甜被发现能通过迷走神经刺激胰岛素分泌,而三氯蔗糖和糖精则对肠道菌群的影响更为显著。这种差异性意味着"人工甜味剂"不应被视为一个同质化的类别。
对于普通消费者而言,适度使用人工甜味剂是安全的,但将其作为健康生活方式的替代品则可能过于乐观。无论是糖还是甜味剂,过量摄入都可能带来问题。真正的健康策略或许应该是逐步减少对甜味的依赖,而不是简单地用一种甜味物质替代另一种。
参考文献
- Zhang Juen et al. The structure of human sweetness. Cell. 2025;188(15):4141-4153.
- Suez J et al. Artificial sweeteners induce glucose intolerance by altering the gut microbiota. Nature. 2014;514(7521):181-186.
- Wu W et al. Sweetener aspartame aggravates atherosclerosis through insulin-triggered inflammation. Cell Metabolism. 2025;37(5):1075-1088.
- WHO. Aspartame hazard and risk assessment results released. 2023.
- Zhang F et al. Characterization of the Binding Site of Aspartame in the Human Sweet Taste Receptor. J Mol Neurosci. 2015;56(4):837-847.
- Pepino MY et al. Sucralose affects glycemic and hormonal responses to an oral glucose load. Diabetes Care. 2013;36(9):2530-2535.
- Swithers SE, Davidson TL. A role for sweet taste: calorie predictive relations in energy regulation by rats. Behav Neurosci. 2008;122(1):161-173.
- FDA. Aspartame and Other Sweeteners in Food. 2025.